شیمی - بازرسی فنی
وبلاگ هر هفته یک حدیث به آدرس www.hadis89.blogsky.com منتظر مشتاقان احادیث پیامبر و ائمه معصومین (ع) می باشد.شیمی - بازرسی فنی
وبلاگ هر هفته یک حدیث به آدرس www.hadis89.blogsky.com منتظر مشتاقان احادیث پیامبر و ائمه معصومین (ع) می باشد.تجزیه عنصری
تجزیه عنصری

برای اکسیژن آزمایش ساده ای وجود نداردو عناصر دیگر با پیوند کوالانسی در اتصال هستندو بنابراین با آزمایش های یونی معمولی مستقیما جواب نمی دهند.ولی اگر جسم آلی مجهول با سدیم مذاب ذوب شود در اگثر موارد طوری ترکیب می شود که NوSوXآن به یونهای CNوSوCNSوXتبدیل می شود.پس از آنکه سدیم اضافی دقیقا از بین برده شد محلول آبی را که محتوی این یونهاست به روش معمولی معدنی تجزیه می کنند.توضیح کامل تری در این مورد وجود دارد که در زیر به آن می پردازیم.
کربن هیدروژن واکسیژن
برای اثبات وجود کربن و هیدروژن نمونه رابا پودر خشک مس(II) اکسید حرارت داده که منجر به ایجاد کربن دی اکسید وآب می شود . حضور کربن در نمونه با عبور دادن گاز های ایجاد شده از درون محلول با ریم یا کلسیم هیدروکسید مشخص نمی شود که دراین صورت رسوب کربنات مربوطه حاصل می شود . هیدروژن را می توان با ایجاد قطره های آب متراکم شده روی قسمت بالایی لوله تشخیص داد . هیچ آزمایش کیفی برای اثبات وجود اکسیژن در ترکیبات آلی وجود ندارد برای تعیین اکسیژن باید تجزیه کمی صورت بگیرد .دراین روش اگر اگر مجموع درصد تمام عناصر تشکیل دهنده ترکیب کمتر آن تا 100 مربوط به در صداکسیژن است .
نیتروژن گوگرد و هالوژن ها
Sustainable Electrodes for Solar Cells

Sustainable Electrodes for Solar Cells
To generate solar energy, a solar cell must have an electrode that is transparent. Currently there are two materials which meet this requirement: indium tin oxide (ITO), which is the preferred one, and fluorine tin oxide (FTO), which is less effective. However, indium is rare and has to be extracted from zinc and lead ores, of which it is a minor component; production is less than 500 tons a year.
ITO and FTO are not without their drawbacks. They lack transparency with respect to the infrared region of the spectrum, and this restricts their ability to gather a wider range of solar energy. They are unstable in the presence of acids and bases, and their metal ions are prone to diffusing into the polymer layers thereby reducing efficiency. Unless they are structurally perfect they suffer from current leakage
ادامه مطلب ...درجه پیچیدگی پالایشگاه و ارزش افزوده فراوردهها
یکی از عواملی که در نحوة عملکرد یک پالایشگاه، میزان ارزش افزوده فراوردههای پالایشی و میزان سوددهی آن تاثیر دارد، درجه پیچیدگی یا قابلیت تولید فراوردههای سبک و با ارزش افزودة بالاتر توسط آن پالایشگاه است. در متن زیر علاوه بر معرفی انواع پالایشگاه از نظر پیچیدگی، به بیان مفهوم پیچیدگی، ضریب پیچیدگی و فرایندهای تبدیل اولیه و ثانویه پالایش میپردازیم:
انواع پالایشگاه از نظر پیچیدگی
میزان سوددهی یک پالایشگاه، به عوامل زیر بستگی دارد: "قیمت نفتخام و در دسترسبودن آن"، "خصوصیات بازار منطقهای"، "ظرفیت فرایندهای پالایشگاه"، "درجه پیچیدگی" و "کارآیی پالایشگاه". انتخاب درجه پیچیدگی مناسب برای یک پالایشگاه، با توجه به این عوامل تعیین میگردد. پالایشگاهها از نظر پیچیدگی به چهار نوع زیر تقسیم میشوند:
1. ساده (Topping)
در این پالایشگاه نفتخام توسط تقطیر اتمسفری، تنها به اجزای تشکیلدهندهاش تبدیل میشود. محصول آن نفتا است و بنزین تولید نمیکند.
2. Hydroskimming
این نوع پالایشگاه به واحد تقطیر اتمسفری و واحد تغییر شکل نفتا (Reforming) مجهز است. از نوع ساده پیچیدهتر است و بنزین تولید میکند. اما مقدار زیادی سوخت کمارزش که تقاضا برای آن کم است، نیز تولید میکند.
3. Cracking
علاوه بر واحدهای ذکر شده در انوع 1 و 2 ، شامل واحد تقطیر خلأ و واحد شکست کاتالیستی (FCC) نیز میباشد. نسبت به نوع 2، یک درجه پیچیدگی بیشتری دارد. تولید نفت کوره در آن کاهش یافته و تبدیل آن به فرآوردههای تقطیر سبک و میانتقطیر انجام میشود.
4. Coking
این پالایشگاه مجهز به فرایندDelayed Coking است که قبل از فرایند شکست کاتالیستی انجام میشود. درجه بالای تبدیل نفت کوره به فراوردههای تقطیر و کک نفت باعث میشود نسبت به انواع قبلی بالاترین پیچیدگی را داشته باشد.
برای نشان دادن میزان پیچیدگی یک پالایشگاه، از ضریب پیچیدگی نلسون استفاده میکنند که این ضریب برای پالایشگاه Hydroskimming، در حدود 2، برای پالایشگاه Cracking تا 5 و برای نوع Coking بالاتر از 9 تعیین شدهاست.
ضریب پیچیدگی پالایشگاه، اطلاعاتی راجع به پیچیدگی پالایشگاه، هزینههای جایگزینی و توانایی ارزشافزوده یک پالایشگاه در اختیار قرار میدهد؛ ضمن اینکه میتوان براساس آن پالایشگاههای مختلف را طبقهبندی کرد.
معرفی فرایندهای پالایش
نوع فرایندهای مورد استفاده در پالایشگاه، در تعیین پیچیدگی آن مؤثر است و هر اندازه واحدهای تبدیل ثانویه یک پالایشگاه، بیشتر باشند درجه پیچیدگی آن نیز بیشتر خواهد بود. در زیر واحدهای تبدیل اولیه و ثانویه و انواع آنها معرفی میشوند:
الف) فرایندهای تبدیل اولیه (Primary Conversion Processes)
1. تقطیر اتمسفری
نانوتکنولوژی

نانوتکنولوژی تولید کارآمد مواد و دستگاهها و سیستمها با کنترل ماده در مقیاس طولی نانومتر و بهره برداری از خواص و پدیدههای نو ظهوری است که در مقیاس نانو توسعه یافتهاند.
یک نانومتر چقدر است؟ یک نانومتر یک میلیاردم متر (10-9 m) است. این مقدار حدودا چهار برابر قطر یک اتم است. مکعبی با ابعاد 2.5 نانومتر ممکن است حدود 1000 اتم را شامل شود. کوچکترین آی سیهای امروزی با ابعادی در حدود 250 نانومتر در هر لایه به ارتفاع یک اتم ، حدود یک میلیون اتم را در بردارند. در مقایسه یک جسم نانومتری با اندازهای حدود 10 نانومتر ، هزار برابر کوچکتر از قطر یک موی انسان است.
امکان مهندسی در مقیاس مولکولی برای اولین بار توسط ریچارد فاینمن (R.Feynnman) ، برنده جایزه نوبل فیزیک مطرح شد. فاینمن طی یک سخنرانی در انستیتو تکنولوژی کالیفرنیا در سال 1959 اشاره کرد که اصول و مبانی فیزیک امکان ساخت اتم به اتم چیزها را رد نمیکند. وی اظهار داشت که میتوان با استفاده از ماشینهای کوچک ماشینهایی به مراتب کوچکتر ساخت و سپس این کاهش ابعاد را تا سطح خود اتم ادامه داد.
همین عبارتهای افسانه وار فاینمن راهگشای یکی از جذابترین زمینههای نانو تکنولوژی یعنی ساخت روباتهایی در مقیاس نانو شد. در واقع تصور در اختیار داشتن لشکری از نانو ماشینهایی در ابعاد میکروب که هر کدام تحت فرمان یک پردازنده مرکزی هستند، هر دانشمندی را به وجد میآورد. در رویای دانشمندانی مثل جی استورس هال (J.Storrs Hall) و اریک درکسلر (E.Drexler) این روباتها یا ماشینهای مونتاژکن کوچک تحت فرمان پردازنده مرکزی به هر شکل دلخواهی در میآیند. شاید در آیندهای نه چندان دور بتوانید به کمک اجرای برنامه ای در کامپیوتر ، تخت خوابتان را تبدیل به اتومبیل کنید و با آن به محل کارتان بروید.
چرا این مقیاس طول اینقدر مهم است؟
خواص موجی شکل (مکانیک کوانتومی) الکترونهای داخل ماده و اثر متقابل اتمها با یکدیگر از جابجاییمواد در مقیاس نانومتر اثر میپذیرند. با تولید ساختارهایی در مقیاس نانومتر ، امکان کنترل خواص ذاتی مواد ازجمله دمای ذوب ، خواص مغناطیسی ، ظرفیت بار و حتی رنگ مواد بدون تغییر در ترکیب شیمیایی بوجود میآید. استفاده از این پتانسیل به محصولات و تکنولوژیهای جدیدی با کارآیی بالا منتهی میشود که پیش از این میسر نبود.
نظام سیستماتیک ماده در مقیاس نانومتری ، کلیدی برای سیستمهای بیولوژیکی است. نانوتکنولوژی به ما اجازه میدهد تا اجزاء و ترکیبات را داخل سلولها قرار داده و مواد جدیدی را با استفاده از روشهای جدید خود_اسمبلی بسازیم. در روش خود_اسمبلی به هیچ روبات یا ابزار دیگری برای سرهم کردن اجزاء نیازی نیست. این ترکیب پر قدرت علم مواد و بیوتکنولوژی به فرآیندها و صنایع جدیدی منتهی خواهد شد.
ساختارهایی در مقیاس نانو مانند نانو ذرات و نانولایهها دارای نسبت سطح به حجم بالایی هستند که آنها را برای استفاده در مواد کامپوزیت ، واکنشهای شیمیایی ، تهیه دارو و ذخیره انرژی ایدهال میسازد. سرامیکهای نانوساختاری غالبا سختتر و غیرشکنندهتر از مشابه مقیاس میکرونی خود هستند. کاتالیزورهای مقیاس نانو راندمان واکنشهای شیمیایی و احتراق را افزایش داده و به میزان چشمگیری از مواد زائد و آلودگی آن کم میکنند. وسایل الکترونیکی جدید ، مدارهای کوچکتر و سریعتر و … با مصرف خیلی کمتر میتوانند با کنترل واکنشها در نانوساختار بطور همزمان بدست آیند. اینها تنها اندکی از فواید و مزایای تهیه مواد در مقیاس نانومتر است.
منافع نانوتکنولوژی چیست؟
مفهوم جدید نانوتکنولوژی آنقدر گسترده و ناشناخته است که ممکن است روی علم و تکنولوژی در مسیرهای غیرقابل پیش بینی تأثیر بگذارد. محصولات موجود نانوتکنولوژی عبارتند از: لاستیکهای مقاوم در برابر سایش که از ترکیب ذرات خاک رس با پلیمرها بدست آمدهاند، شیشههایی که خودبه خود تمیز میشوند، مواد دارویی که در مقیاس نانو ذرات درست شدهاند، ذرات مغناطیسی باهوش برای پمپهای مکنده و روان سازها ، هد دیسکهای لیزری و مغناطیسی که با کنترل دقیق ضخامت لایهها از کیفیت بالاتری برخوردارند، چاپگرهای عالی با استفاده از نانو ذرات با بهترین خواص جوهر و رنگ دانه و ... .
قابلیتهای محتمل تکنیکی نانوتکنولوژی
محصولات خود_اسمبل
کامپیوترهایی با سرعت میلیاردها برابر کامپیوترهای امروزی
اختراعات بسیار جدید (که امروزه ناممکن است)
سفرهای فضایی امن و مقرون به صرفه
نانوتکنولوژی پزشکی که در واقع باعث ختم تقریبی بیماریها ، سالخوردگی و مرگ و میر خواهد شد.
دستیابی به تحصیلات عالی برای همه بچههای دنیا
احیاء و سازماندهی اراضی
برخی کاربردها
فرآیند مشعل پالایشگاه
مجموعه مشعل پالایشگاه واحدی است که جهت ایمن سازی محیط پالایشگاه و واحدهای بهره برداری طراحی و نصب شده است.
کاربرد اساسی آن مهار کردن و به کنترل درآوردن شرایط غیرقابل کنترلی است که دراثربالا رفتن بیش ازحد مجازعملیاتی دردستگاههای پالایش بوجود می آید. کنترل فوق از طریق تخلیه گازمازاد واحدها به شبکه مشعل انجام می گیرد.
این مجموعه شامل قسمتهای زیر می باشد:
1. لوله های رابط واحد
2. لوله اصلی (BLOW DOWN) مشعل که از محوطه بارگیری گاز مایع شروع شده و تا ستونهای مشعل امتداد دارد.
3. ظروف مایع گیر بین راهی (K.O.DROM)
4. تلمبه های تخلیه مایعات جمع شده در ظروف بین راهی
5. ستونهای اصلی مشعلها .
۶. دستگاه جرقه زن الکتریکی برای روشن کردن مشعلها
خروجی تمام شیرهای ایمنی، لوله های تخلیه(DRAIN) و تهویه (VENT) ظروف برج ها، تلمبه ها ،کمپرسورها ،اعم از گازی یا مایع(به استثناء آب ،بخار،هوای فشرده، ازت ) توسط لوله های تخلیه فشار هر واحد جمع آوری شده به لوله اصلی مشعل منتقل می گردند.
قسمت عمده مایعات همراه با گازها در ظروف مایع گیر بین راهی جداشده و گازها وارد محفظه آب بندی در پائین مشعل می گردند،پس از شستشو و حذف ذرات و مایعات احتمالی توسط آب برای سوختن به بالای مشعل هدایت و درتاج (TIP) مشعل می سوزند.
ایزومرها در شیمی فضایی
یک بخش از شیمی فضایی ، ایزومری فضایی است. ایزومرها ترکیبات متفاوتی هستند که فرمول مولکولی یکسانی دارند. ایزومرهای خاصی که فقط از نظر جهت گیری اتمها در فضا باهم تفاوت دارند اما از نظر نحوه اتصال اتمها به یکدیگر ، شبیه یکدیگرند، ایزومرهای فضایی نام دارند.
شباهت و تفاوت ایزومرهای فضایی
تفاوت جفت ایزومرهای فضایی از نظر ساختار و بنابراین از نظر خواص بسیار کوچک است. اما از نظر همه خواص فیزیکی قابل سنجش ، با یکدیگر مشابهند مگر از نظر تاثیر بر نوعی نور غیر عادی. با استفاده از همین تاثیر متفاوت و دستگاه خاص مربوطه میتوان دو ایزومر را از یکدیگر باز شناخت.
کاربرد متفاوت ایزومرهای فضایی
با وجود شباهت نزدیک ، وجود اینگونه ایزومرها ، یکی از سنجشگرهای بسیار حساس را برای تشخیص مکانیسم واکنشها در اختیار شیمیدان میگذارد. غالبا یکی از این ایزومرها برای مطالعه برگزیده میشود. نه به این دلیل که این ایزومرها از نظر شیمی سه بعدیاش با ترکیبهای دیگر فرق دارد، بلکه به این دلیل که این ترکیب میتواند نکتههایی را آشکار سازد که در ترکیبهای عادی پنهاناند و باز هم با وجود شباهت نزدیک دو ایزومر فضایی ، ممکن است یکی از آنها یک غذای مقوی یا یک آنتی بیوتیک یا یک داروی محرک قلب باشد، ولی ایزومر دیگر ترکیبی بیمصرف باشد.
تعداد ایزورمها و کربن چهار وجهی
باید در نظر داشت که هر ترکیبی ولو پیچیده که دارای کربنی متصل به چهار اتم دیگر است را میتوان مشتقی از متان تلقی کرد و آنچه که درباره شکل مولکول متان فرا میگیریم را میتوانیم درباره شکل مولکولهای پیچیده بکار بریم. برای هر اتم ، فقط یک ماده با فرمول یافت شده است. با کلردار کردن متان ، فقط یک ترکیب با فرمول و با برمدار کردن آن فقط یک ترکیب با فرمول بدست میآید. به همین ترتیب فقط یک و یک شناخته شده است.
در واقع ، اگر ، بجای اتم نمایاننده یک گروه از اتمها باشد نیز مطلب فوق صادق است، مگر هنگامی که گروه تا آن حد پیچیده است که خود سبب ایزومری میشود. به عنوان مثال فقط یک ، یک و یک وجود دارد. این نشان میدهد که در متان ، همه اتمهای هیدروژن هم ارزند، بطوری که با جایگزین کردن هر کدام از آنها ، فرآورده یکسانی حاصل میشود. اگر اتمهای هیدروژن متان هم ارز نبودند، با جایگزین کردن هر کدام از آنها ترکیب متفاوتی بدست میآمد و فرآوردههای استخلافی ایزومری حاصل میشدند.
برای اتمهای هیدروژن در متان سه آرایش امکان پذیر است که هم ارز باشند:
آرایش مسطح که در آن اتم کربن در مرکز یک مستطیل یا مربع و اتمهای هیدروژن در چهار گوشه آن قرار دارند.
آرایش هرمی که در آن اتم کربن در راس هرم و اتمهای هیدروژن در چهار گوشه آن قرار دارند.
آرایش چهار وجهی که در آن کربن در مرکز چهار وجهی و هر اتم هیدروژن در یک گوشه آن است.
فعالیت نوری
نور خواصی دارد که با در نظر گرفتن آن به عنوان یک پدیده موجی بخوبی درک میشوند. موجی که در آن ارتعاشها بصورت عمود بر جهت حرکت نور روی میدهند. تعداد سطحهایی که از خط مسیر نور میگذرند بیشمارند و نور معمولی در همه این سطوح در حال ارتعاش است. اگر مستقیما به باریکهای از نور یک لامپ بنگریم، نوع ارتعاشهایی که روی میدهند و همگی عمود بر خط بین چشمان ما و منبع نور (لامپ) هستند را نشان میدهد.
نور معمولی ، با عبور کردن از یک عدسی ساخته شده از مادهای به نام "پلاروید" یا از یک قطعه کلسیت (نوعی بلور ) با آرایشی که به نام منشور نیکول معروف است، به نور قطبیده در سطح تبدیل میشود. یک ماده فعال نوری ، مادهای است که سطح نور قطبیده را میچرخاند. وقتی نور قطبیده در حال ارتعاش در یک سطح معین ، از میان یک ماده فعال نوری میگذرد، در حال ارتعاش در یک سطح دیگر پدیدار میشود.
پلاریمتر
الکترونگاتیویته چیست ؟
متداولترین مقیاس الکترونگاتیویته
مقیاس نسبی الکترونگاتیوی پاولینگ ، متداولترین مقیاس و مبتنی بر مقادیر تجربی انرژیهای پیوندی است. مقدار انرژی اضافی که از جاذبه متقابل بارهای جزئی б+ و б- اضافه بر انرژی پیوند کووالانسی آزاد میشود، به قدر مطلق б و به تفاوت الکترونگاتیوی دو عنصر پیوند شده بستگی دارد. در محاسبات الکترونگاتیوی تنها تفاوت الکترونگاتیویته عناصر تعیین میشود. برای بنا کردن یک مقیاس ، به اتم F (الکترونگاتیوترین عنصر) بطور دلخواه عدد 4 نسبت داده شده است.
مقیاس الکترونگاتیوی پاولینگ ، متداولترین مقیاس و مبتنی بر مقادیر تجربی انرژیهای پیوند است. مثلا انرژی پیوند Br-Br ، انرژی لازم برای تفکیک مولکول Br2 به اتمهای Br است. برای تفکیک یک مول از مولکولهای Br2 به اندازه 46+ کیلو کالری انرژی لازم است. انرژی پیوند H-H برابر 104+ کیلو کالری بر مول است.
تعاریف مختلف الکترونگاتیویته
الکترونگاتیویته ، در روشهای متفاوتی تعریف شده است که برخی از آنها به اختصار توضیح داده میشود.
الکترونگاتیویته پاولینگ
انرژی اضافی پیوند A-B نسبت به متوسط انرژی پیوندهای A-A و B-B میتواند به حضور سهم یونی در پیوند کوالانسی نسبت داده شود. اگر انرژی پیوند A-B بطور قابل ملاحظه ای از متوسط پیوندهای غیر قطبی A-A و B-B متفاوت باشد، میتوان فرض کرد که سهم یونی در تابع موج و بنابراین اختلاف بزرگ در الکترونگاتیوی وجود دارد.
الکترونگاتیویته آلرد_روکر در این تعریف ، الکترونگاتیویته توسط میدان الکتریکی بر سطح اتم مشخص میشود. بنابرین الکترون در یک اتم بار موثر هستهای را احساس میکند. بر طبق این تعریف ، عناصری با الکترونگاتیویته بالا آنهایی هستند که با بار هستهای موثر بزرگ و شعاع کوالانسی کوچک ، این عناصر در نزدیکی فلوئور قرار دارند.
الکترونگاتیویته مولیکن مولیکن تعریف خود را بر پایه دادههای طیفهای اتمی نهاد. او فرض کرد که توزیع دوباره الکترون در طی تشکیل تر کیب به گونهای است که در آن یک اتم به کاتیون (توسط ار دست دادن الکترون) و اتم دیگر به آنیون (توسط گرفتن الکترون) تبدیل میشود.
اگر یک اتم دارای انرژی یونیزاسیون بالا و الکترونخواهی بالا باشد، احتمالا در هنگام تشکیل پیوند ، الکترونها را به سوی خود میکشد. بنابراین بعنوان الکترونگاتیو شناخته میشود. از طرف دیگر اگر انرژی یونش و الکترونخواهی آن ، هر دو کوچک باشد تمایل دارد تا الکترون از دست بدهد. بنابراین به عنوان الکترو پوزیتیو طبقه بندی میشود.
این مشاهدات تعریف مولیکن را به عنوان مقدار متوسط انرژی یونش و الکترونخواهی عنصر معرفی میکند.
تغییرات الکترونگاتیویته عناصر
الکترونگاتیویته عناصر با افزایش تعداد الکترونهای والانس و همچنین کاهش اندازه اتم افزایش مییابد و در هر دوره از جدول تناوبی از چپ به راست و در هر گروه از پایین به بالا افزایش مییابد. فلزات ، جاذبه کمی برای الکترونهای والانس دارند و الکترونگاتیوی آنها حاکم است، ولی نافلزات ، به استثنای گازهای نجیب ، جاذبه قوی برای اینگونه الکترونها دارند و الکترونگاتیوی آنها زیاد است.
بطور کلی ، الکترونگاتیوی عناصر در هر دوره از چپ به راست (با افزایش تعداد الکترونهای والانس) و در هر گروه از پایین به بالا (با کاهش اندازه اتم) افزایش مییابد. بنابراین ، الکترونگاتیوترین عناصر ، در گوشه بالایی سمت راست جدول تناوبی (بدون در نظر گرفتن گازهای نجیب) و عناصری که کمترین الکترونگاتیوی را دارند، در گوشه پایینی سمت چپ این جدول قرار دارند. این سیر تغییرات ، با سیر تغییرات پتانسیل یونش و الکترونخواهی عناصر در جدول تناوبی همجهت است.
مفهوم الکترونگاتیوی
مفهوم الکترونگاتیوی گرچه مفید است، ولی دقیق نیست. روشی ساده و مستقم برای اندازه گیری خاصیت الکترونگاتیویته وجود ندارد و روشهای گوناگون برای اندازه گیری آن پیشنهاد شده است. در واقع چون این خاصیت علاوه بر ساختمان اتم مورد نظر به تعداد و ماهیت اتمهای متصل به آن نیز بستگی دارد، الکترونگاتیوی یک اتم نامتغیر نیست.
انتظار میرود که الکترونگاتیوی فسفر در PCl3 با الکترونگاتیوی آن در PCl5 تفاوت داشته باشد. از اینرو ، این مفهوم را تنها بایستی نیمهکمی تلقی کرد. بنابراین میتوان گفت که قطبی بودن مولکول HCl ناشی از اختلاف بین الکترونگاتیوی کلر و هیدروژن است چون کلر الکترونگاتیوتر از هیدروژن است، آن سر مولکول که به کلر منتهی میشود، سر منفی دو قطبی است.
توجیه پیوند یونی با خاصیت الکترونگاتیویته
پیوند یونی بین غیرفلزات وقتی تشکیل میشود که اختلاف الکترونگاتیوی آنها خیلی زیاد نباشد. در اینگونه موارد، اختلاف الکترونگاتیوی عناصر نشان دهنده میزان قطبی بودن پیوندهای کووالانسی است. اگر اختلاف الکترونگاتیوی صفر یا خیلی کوچک باشد، میتوان گفت که پیوند اساسا غیر قطبی است و اتمهای مربوط ، سهم مساوی یا تقریبا مساوی در الکترونهای پیوند دارند.
هر چقدر اختلاف الکترونگاتیوی بیشتر باشد پیوند کووالانسی قطبیتر خوهد بود (پیوند در جهت اتم الکترونگاتیوتر قطبی میشود). بنابراین با توجه به مقادیر الکترونگاتیوی میتوان پیشگویی کرد که HF قطبیترین هیدروژن هالیدها است و انرژی پیوندی آن بیشتر از هر یک از این ترکیبات است. البته نوع پیوندی که بین دو فلز تشکیل میشود، پیوند فلزی و در آن اختلاف الکترونگاتیوی نسبتا کم است.
کاربردهای الکترونگاتیویته
میتوان برای تعیین میزان واکنش پذیری فلزات و غیر فلزات بکار برد.
میتوان برای پیشبینی خصلت پیوندهای یک ترکیب بکار برد. هرچه اختلاف الکترونگاتیوی دو عنصر بیشتر باشد، پیوند بین آنها قطبیتر خواهد بود. هرگاه اختلاف الکترونگاتیوی دو عنصر در حدود 1.7 باشد، خصلت یونی نسبی پیوند بیش از 50% است.
اگر اختلاف الکترونگاتیوی صفر و یا خیلی کوچک باشد، پیوند غیر قطبی است. هرچه اختلاف الکترونگاتیوی بیشتر باشد، پیوند کووالانسی قطبیتر خواهد بود. در این پیوندها ، اتمی که الکترونگاتیوی بیشتری دارد، بار منفی جزئی را خواهد داشت.
با استفاده از مقادیر الکترونگاتیوی میتوان نوع پیوندی را که یک ترکیب ممکن است داشته باشد، پیشبینی کرد. وقتی دو عنصر با اختلاف الکترونگاتیوی زیاد با یکدیگر ترکیب می شوند، یک ترکیب یونی حاصل میشود. مثلا اختلاف الکترونگاتیوی سدیم و کلر 2.1 است و NaCl یک ترکیب یونی است.
آیا الکترونگاتیوی یک عنصر همیشه ثابت است؟
مفهوم الکترونگاتیوی غیر دقیق است. زیرا این خاصیت نه تنها به ساختمان اتم مورد بحث بستگی دارد، بلکه تعداد و ماهیت اتمهای دیگری که به اتم مزبور پیوند داده شدهاند نیز در آن دخالت دارد. بنابراین الکترونگاتیوی یک عنصر همیشه ثابت نیست مثلا الکترونگاتیوی فسفر در ترکیب (PCl3) متفاوت از الکترونگاتیوی آن در ترکیب (PCl5) است.
فرآیند پالایشگاه
فرآیند پالایشگاه
گازهای سوختی - گازهایمایع - انواع بنزین - سوختهای توربین گازی (جت) - نفت سفید - فراورده های میان تقطیر (سوخت دیزل و نفت کوره های سبک) - نفت کوره باقیمانده ای - روغنهای روانساز - روغنهای سفید - فراورده های میان روغنهای ترانسفورماتور و کابل- گریس- مومها (واکس) - آسفالتها - ککها - دودهها - مواد شیمیایی ، حلالها ، متفرقه.
منابع خوراک پالایشگاه
مواد خام پایه پالایشگاهها نفت خام است. اگر چه در بعضی موارد از نفتهای سنتزی حاصل از سایر منابع (جیلسوتیت، ماسههای قیری ، غیره) نیز استفاده میشود.
فرایندهای پالایش در پالایشگاه
تقطیر نفت خام
دستگاههای تقطیر نفت خام ، نخستین واحدهای فراورش (پالایش) عمده در پالایشگاه هستند. تفکیک نفت خام در دو مرحله صورت میگیرد، اول تفکیک جزء به جزء همه نفت خام در فشار اتمسفر و سپس ارسال باقیمانده دیر جوش این مرحله به دستگاه تفکیک دیگری که تحت خلاء شدید عمل میکند. بنابراین ، نفت خام پس از حرارت در کوره در برج تقطیر اتمسفری به فراوردههای زیر تفکیک میشود:
گازهای سوختی ( که عمدتا شامل متان و اتان است ) ، گازهای سبکتر (شامل پروپان ، بوتان و همچنین متان و اتان است) ، نفتهای سبک تثبیت نشده ، نفتهای سنگین ، نفت سفید ، نفت گاز اتمسفری و باقیمانده خام برج تقطیر اتمسفری (ARC). در برج تقطیر در خلاء نیز باقیمانده برج تقطیر اتمسفری به جریان نفت گاز خلاء و باقیمانده برج تقطیر در خلاء (VRC ) تفکیک میشود. نفت گاز اتمسفری و نفت گاز خلاء را غالبا برای تولید بنزین ، سوخت هواپیما و سوخت دیزل به واحد هیدروکراکینگ یا کراکینگکاتالیزی میفرستند.
باقیمانده برج خلاء را نیز میتوان در واحدهای گرانروی شکن ، کمکسازی و یا آسفالتزدایی برای تولید نفت کوره سنیگن و یا خوراک واحد کراکینگ و یا مواد خام روغن روانسازی پالایش کرد. باقیمانده نفت خامهای آسفالتی را میتوان برای تولید آسفالت جاده سازی و یا پشت بام ، مورد عملیات یا پالایش دیگری قرار داد.
فرایندهای کک سازی و گرمایی
باقیمانده خام برج تقطیر در خلاء ( VRC ) در واحد کک سازی به کمک گرما شکسته میشود و در نتیجه گاز تر، بنزین واحد کک سازی ، نفت گاز واحد کک سازی و کک تولید میشود. در واقع ، در کک بدست آمده مواد فرار و یا با نقطه جوش بالا وجود دارد. برای حذف اغلب مواد فرار از کک نفتی ، باید آن را در دمای 2000 تا 2300 درجه فارنهایت تکلیس کرد. موارد استفاده اصلی از کک نفتی عبارتند از:
سوخت انواع کورهها ، ساخت آند ها برای کاهش سلول الکترولیتی آلومین ، استفاده مستقیم از آن به عنوان منبع کربن شیمیایی برای تولید فسفر عنصری ، کلسیم کاربید و سیلسیم کاربید ، ساخت الکترود برای بکارگیری در کوره الکتریکی تولید فسفر عنصری ، تیتان دی اکسید ، کلسیم کاریبد و سیلیسیم کاربید ، تولید گرافیت.

کراکینگ و هیدروکراکینگ کاتالیزی
نفت گاز حاصل از واحدهای تقطیر اتمسفری و تقطیر در خلاء و کک سازی به عنوان خوراک واحدهای کراکینگ کاتالیزوری و یا هیدروکراکینگ بکار میرود. این واحدها مولکولهای سنگین را شکسته و آنها را به مواد باارزشتری مانند بنزین ، سوخت جت و نفت کوره سبک تبدیل میکنند. فراورده های سیر نشده واحد کراکینگ ، نخست سیر میشوند و سپس در واحد تبدیل و یا واحد پالایش با هیدروژن ، کیفیت بهتری پیدا میکنند. فراورده های واحد هیدروکراکینگ ، سیر شده هستند.
رفرمینگ (تبدیل) کاتالیزی و همپارش
نیاز اتومبیلهای امروزی به بنزینهای با عدد اکتان بالا ، محرکی برای استفاده رفرمینگ کاتالیزی شد. در رفرمینگ کاتالیزی ، تغییر در نقطه جوش مادهای که از این واحد میگذرد، نسبتا کم است، زیرا مولکولهای هیدروکربن ، شکسته نمیشوند، بلکه ساختارهای آنها بازآرایی میشوند تا آروماتیکهای با عدد اکتان بالا تولید شوند. منابع خوراک واحد رفرمینگ کاتالیزی عبارتند از:
بنزینهای سنگن تقطیر مستقیم (HSR ) و نفت سنگین حاصل از واحدهای برج تقطیر نفت خام ، کک سازی و کراکینگ. فراوده های حاصل تبدیل کاتالیزی برای فروش به عنوان بنزین معمولی و بنزین ******** با هم مخلوط میشوند.
عدد اکتان نفتهای سبک ( LSR ) را میتوان با استفاده از فرایند همپارش که طی آن پارافینهای نرمال (راست زنجیر) به همپارهایشان تبدیل میشوند، بهبود بخشید.
بازیابی بخار (واحد صنعتی گاز)
جریانهای گاز تر حاصل از واحد تقطیر نفت خام ، کک سازی و واحدهای کراکینگ در بخش بازیابی بخار ، به گاز سوختی ، گاز نفتی مایع ( LPG ) ، هیدروکربنهای سیر نشده (پروپیلن، انواع بوتیلن و پنتن )، نرمال بوتان و ایزوبوتان تفکیک میشوند. گاز سوختی در کورههای پالایشگاه سوزانده میشود و n-بوتان با بنزین و یا LPG مخلوط میشود. هیدروکربنهای سیر نشده و ایزوبوتان بمنظور فراورش ، به واحدهای آلکیل دار شدن فرستاده میشوند.
آلکیل دار کردن
افزایش یک گروه آلکیل به هر ترکیب ، یک واکنش آلکیل دار کردن است. ولی در پالایش نفت ، واژه آلکیل دار کردن در مورد واکش اولفین های دارای وزن مولکولی پایین با یک ایزوپارافین ، به منظور تشکیل ایزوپارافینهای دارای وزن مولکولی بالاتر ، بکار می رود. نیاز به سوختهای هواپیمایی با عدد اکتان بالا انگیزه خوبی برای توسعه فرایند آلکیل دار کردن بمنظور تولید بنزینهای ایزوپارافینی با عدد اکتان بالا بود.
اگر چه آلکیل دار کردن در فشار و دمای بالا ، بدون نیاز به کاتالیزگر مسیر است، ولی تنها فرایندهایی از اهمیت اقتصادی برخورد دارند که در دمای پایین و در مجاورت سولفوریک اسید یا هیدروفلوئوریک اسید انجام می شود. با انتخاب مناسب شرایط عملیاتی ، بیشتر فراوردهها در گستره جوش بنزین با اعداد اکتان موتوری 88 تا 94 و اعداد اکتان پژوهشی بین 94 تا 99 قرار میگیرد.
الکل Alcohol
الکل Alcohol

در شیمی به هر ترکیب شیمیایی که یک گروهِ هیدروکسیل (-OH) متصل به کربن یک آلکیل داشتهباشد، الکل گویند. فرمول کلی یک الکل سادهٔ عیر حلقهای CnH2n+1است. در شیمی الکلها در شمار گروه مهمی از ترکیبهای شیمیایی هستند و در واکنشهای گستردهای شرکت میکنند و بسیاری از ترکیبهای شیمیایی از آنها به دست میآیند، به طوری در کتاب شیمی آلی موریسن و بوید آمدهاست که اگر به شیمیدانی بگویند او را با ده ترکیب شیمیایی دریک جزیره تنها خواهند گذاشت الکل یکی از آنها خواهدبود.
به طور کلی، زمانی که نام الکل به تنهایی به کار میرود، معمولاً منظور اتانول است که همان الکل گرفتهشده از جو یا عرق یا همان مشروبات الکلی میباشد. اتانول مایعی بیرنگ و فرار وبا بویی بسیار تند است که از تخمیر شکرها به دست میآید. همچنین گاه به هر گونه نوشیدنی که الکل داشتهباشد، الکل میگویند. هزاران سال است که معمولاً الکل به عنوان یکی از عاملهای اعتیادآور به شمار میآید.
الکلهای دیگر بیشتر با صفتهای مشخصکنندهٔ ویژهٔ خود میآیند مانند الکل چوب (که همان متانول است) یا ایزوپروپیل الکل. پسوند «ول» نیز در پایان نام شیمیایی همهٔ الکلها میآید
تاریخچه
الکل را نخستین بار ابوبکر محمد بن زکریای رازی پزشک و شیمیدان ایرانی از تقطیر شراب تهیه کرد.[۱] وی آنرا الکحل نامید. بعدها یک آمریکایی بنام دکتر واندیک آن را الکل نامید. گرچه تاریخ تهیه شراب در به هزاران سال پیش در ایران نیز میرسد اما تا زمان رازی کسی الکل را خالص نکرده بود
ریشهشناسی
نظریهٔ غالب بر این است که از آنجا که نخستین بار که زکریای رازی الکل را کشف کرد، آن را با نامِ تازیِ «الکحل» خواند و از آنجا آن را اعراب «الکحول» نامیده و سرانجام در فارسی الکل نام گرفت ولی از آنجا که در عربی «الکحول» نمیتواند از «الکحل» مشتق شدهباشد این احتمال وجود دارد که این واژه از واژهٔ «الغول» که در قرآن آمدهاست گرفته شدهباشد و ریشهای اروپایی داشته باشد.[۲]
ساختار و دستهبندی
الکلها بسته به نوع کربن[۳] که به گروه OH- پیوند دارد، به سه دسته نوع اول ، نوع دوم یا نوع سوم طبقهبندی میشوند:

الکل نوع اول CR(H)۲-OH.
الکل نوع دوم C(R)۲H-OH.
الکل نوع سومC(R)۳-OH.
خواص فیزیکی الکلها
دمای جوش
زغال فعال شده چیست؟
زغال فعال شده چیست؟
اصطلاح زغال فعال شده نشان دهنده یک سری از مواد جذب کننده سطحی , با جنسی زغالی و شکل کریستالی می باشد که در ساختار داخلی آن روزنه های زیادی وجود دارد.
زغال فعال شده دارای کاربردهای زیادی است, از جمله مصارف آن:
- تصفیه آبها ( آب شرب, آب آکواریومها, آبهای صنعتی), از نظر رنگ و بو و طعم
- رنگزدایی از قند و شکر
- بازیافت طلا
- بهسازی رنگ و طعم در نوشیدنی ها و آب میوه ها
- استفاده در دستگاههایی مثل: تصفیه کننده های هوا, خوش بو کننده ها, تصفیه کننده های صنعتی و ...
- ....
تولید زغال فعال شده اصول و فنون گوناگونی در ساخت و تولید زغالهای فعال شده وجود دارد که به 3 اصل بستگی دارد:
- نوع ماده اولیه
- مشخصات فیزیکی مورد نظر برای محصول (زغال فعال شده)
- مشخصات جذبی برای کاربردهای مختلف
شیوه های فعالسازی که بیشتر در تولیدات تجاری بکار میرود عبارتند از:
فعال سازی شیمیایی،فعال سازی توسط بخار
فعال سازی شیمیایی:
ادامه مطلب ...مشتقات غیر هیدروکربنی نفت خام
مشتقات غیر هیدروکربنی نفت خام ، معمولا شامل ترکیبات گوگرددار ، اکسیژندار و ازتدار میباشد. نوع این مشتقات در نفت خام در نوع خود پالایش نفت نیز موثر میباشد. درصد این ترکیبات در نفت زیاد نیست. ترکیبات اکسیژندار و گوگرددار ، تقریبا 2% نفت خام را شامل میشود. البته این درصد قابل تغییر است. این ترکیبات ، بیشتر در برشهای سنگین یافت میشوند و بنابراین حائز اهمیت میباشند.
ترکیبات گوگرددار عملا کلیه نفتهای شناخته شده ، دارای گوگرد هستند. نفتهای بدست آمده از آمریکای جنوبی و خاورمیانه و خاور نزدیک بطور متوسط دارای گوگرد بیشتری است. در نفتهای خام ایران، در حد گوگرد استخراج شده از 1،22% در نفت هفت گل تا 2،46% در نفت خارک تغییر مینماید. نفتهای اروپای شرقی ، خاور دور ، هند ، پاکستان و برمه بطور متوسط از نفتهای خام سایر نقاط ، کم گوگردتر است.
نسبت درصد گوگرد زیاد در اکثر فرآوردههای نفتی ، مضر است و حذف یا تبدیل آنها به مواد بی ضرر ، قسمتهای مهم کار پالایشگاهها را تشکیل میدهد. وجود ترکیبات گوگردی در بنزین ، به علت خورندگی که در قسمتهای موتور ایجاد مینماید، مضر تشخیص داده شده است و مخصوصا در شرایط زمستانی به علت جمع شدن SO2 محلول در آب که در نتیجه احتراق بدست می آید، در محوطه میل لنگ موجب خورندگی بسیار میشود. به علاوه هرکاپتانهای محلول در مواد نفتی ، مستقیما در مجاورت هوا موجب خورندگی مس و برنج میشود. هرکاپتانها همچنین تاثیر نامطلوبی روی حساسیت سرب و ثبات رنگ فرآوردهها دارد. گوگرد آزاد در صورتی که وجود داشته باشد، خورنده است. سولفورها ، دیسولفورها و تیوفنها ، کمتر خورنده هستند؛ اما موجب کم شدن عدد اکتان در مجاورت تترااتیل سرب میشوند.
قسمت اعظم 2 SHدر موقع تقطیر نفت در درجات حرارت 330 و 400 درجه فارنهایت از نفت خارج میشود.
ترکیبات اکسیژندار این ترکیبات 2% ترکیبات نفتی را شامل میشوند و تا 8% افزایش مییابند. برخلاف ترکیبات گوگردار ، ترکیبات اکسیژندار مانند اسیدهای نفتنیک ، در صنعت کاربرد دارند. از نظر اینکه اولین اسیدهای حاصله از نفت ، از مشتقات مونوسیکلوپارافینها (نفتنها) بودهاند، آنها را اسیدهای نفتنیک نام نهادهاند. علاوه بر اسیدهای نفتنیک ، اسیدهای آلیفاتیک نیز در نفت دیده شدهاند. وجود فنلها در چکیدههای کراکینگ ثابت شده و مقدار ناچیزی نیز در بنزین خام مشاهده شده است. به این جهت به نظر میرسد که فنلها در نفت خام وجود داشته باشند. به جز اسیدهای نفتنیک و ترکیبات فنلی ، استرها ، انیدریدها ، الکلها و ستنها و آلدئیدها در نفت مشاهده شدهاند.
تهیه اسیدهای نفتنیک از نفت ، اهمیت تجارتی پیدا کرده و تولید سالانه به شدت افزایش یافته است. این اسیدها به شکل املاح فلزی خود مصرف میشوند. نفتناتهای سرب اهمیت زیادی دارند؛ زیرا به عنوان روغنهای مقاوم (در برابر فشار) و خشک کننده رنگها همراه با نفتنناتهای کبالت و منگنز مصرف میشوند. نفتناتهای مس به عنوان محافظ چوب و در ساختمان رنگهای مختلف مورد استفاده قرار میگیرند. املاح دیگر در گریسها به منظور تهیه گریس مقاوم در مقابل اکسیژن مصرف میشوند.
ترکیبات نیتروژندار یا ازتدار
ترکیبات نیتروژندار ، 50% ترکیبات نفت را شامل میشوند. (نیتروژن به عنون عامل مسموم کننده کاتالیست در شکستن کاتالسیتها میباشد.) در بعضی از نفتها ، نیتروژن وجود ندارد. با وجود مقدار کم ازت در نفت این درصد اهمیت زیادی در پالایشگاهها پیدا میکند، زیرا ترکیبات نیتروژندار را عامل اصلی مسموم کننده کاتالیزور در دستگاههای کراکینگ کاتالسیتی میدانند و نیز تشکیل صمغ را در موقع استفاده از بعضی فرآوردهها از قبیل سوختها ، به ترکیبات ازتدار نسبت میدهند.
ترکیبات ازتدار نفت را به دو گروه قلیایی و قلیایی خاکی تقسیم کردهاند. این تقسیم بندی ، بر مبنای قابلیت ترکیب این مواد با محلول اسید پرکلریک و اسید استیک قرار دارد. از ترکیبات ازتدار موجود در چکیدههای حاصل از دستگاه تقطیر ، 25 الی 35 درصد جزو گروه قلیایی است. ترکیبات ازتدار گروه قلیایی به سادگی از نفت جدا میشوند و به این سبب تحقیقات زیادی روی آنها صورت گرفته است. مشتقات پیریدین و کینولین تنها ترکیبات ازتدار گروه قلیایی است که در محصولات سبک حاصل از دستگاه کراکینگ وجود دارد. از گروه قلیایی میتوانیم از پیریدینها ، کینولینها ، آمینها ، اندولینها و هگزا هیدرو کربازولها نام ببریم. از گروههای غیر قلیایی میتوانیم از پیرولها ، اندولها و کربازولها نام ببریم.
ترکیبات فلزدار در نفت ، علاوه بر ترکیبات مذکور ترکیبات فلزدار هم وجود دارد. در شیمی آلی با این عملکرد روبرو هستیم که برای مطالعه وجود ترکیبات معدنی در ترکیبات آلی معمولا از خاکستر ترکیبات آلی استفاده میشود. در مورد ترکیبات نفتی نیز خاکستر آنها استفاده میشود.
فتوکاتالیست چیست؟
فتو کاتلیست چیست؟ فتو کاتالیست ها مواد پاک کننده محیطی هستند ،هنگامی که نورخورشید و یا فلورسانس به آنها برخورد می کند ازروی سطوح آلودگی ها را بر می دارند و می توانند ترکیبات آلی مثل باسیل ها و بو ها را از بین ببرند. فرایند فتو کاتالیستی از اصول زیر پیروی می کنند.
اصول فرایندفتو کاتالیستی:
1.در معرض اشعه ماورای بنفش UV در زمانی که نور اشعه UV به فتو کاتالیست بر خورد می کند ، الکترون به سطح بالا می آید.در این زمان حفره ای که الکترون از آن بیرون جهیده بود حفره مثبت نامیده می شود . 2.ظهور رادیکال های OHحفره مثبت دارای قدرت اکسیداسیون بالایی است و الکترون را از-OH (یون هیدروکسید )در آب می گیرد.در این زمان- OH،که الکترونش گرفته شده تبدیل به OH رادیکالی می شود که تا حد زیادی ناپایدار است. 3.تخریب ترکیبات آلی OH رادیکالی ،طی یک اکسیداسیون قوی الکترون را از نزدیک ترین ترکیب آلی همسایه دریافت می کند تا به پایداری بیشتری برسد.با این روش ترکیبات آلی با از دست دادن الکترون ودر نهایت تبدیل شدن به دی اکسید کربن و آب تخریب می شود و به اتمسفر بر می گردد. 1.سوال؟>>فتو کاتالیست ها با منبع نور کار می کنند.چه نیازی هست که منبع نور حتما مااورای بنفش باشد؟ TiO2 یک نیمه هادی است که با دریافت انرژی نور به سطوح بالاتری از انرژی بر انگیخته می شود و الکترون ها را از سطح تابش شده رها می سازد.اگر میزان انرژی کافی باشد همه الکترونها از سطح که نوار ظرفیت (Valence band) نامیده می شود به نوار ظرفیت هدایتی Conduction band جهش می یابند.انرژی که به این سطح داده می شود از نوع انرژی نورانی است که مربوط به طول موج نور تابیده می باشد.از میزان جهش الکترونها چنین بر می آید که محدوده تابش نور UV می باشد.
انواع فتو کاتالیست ها:
شناساگرها
اطلاعات اولیه
انواع گوناگونی از ترکیبات ، هم سنتزی و هم طبیعی وجود دارند که بر حسب PH محلولی که در آن حل میشوند، رنگ متفاوتی به خود میگیرند. بعضی از این مواد هزاران سال است که برای نشان دادن خصلت اسیدی یا بازی آبها بکار گرفته شدهاند. این ترکیبات همچنین برای شیمیدان عصر حاضر که از آنها برای تخمین PH محلولها و تشخیص نقطه پایانی در تیتراسیونهای اسید – باز سود میبرند، اهمیت زیادی دارند.
رنگ شناساگر 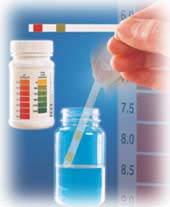
محلولی که محتوی یک شناساگر باشد، با تغییرات PH ، یک تغییر پیوسته در رنگ از خود ظاهر میسازد. لکن ، چشم انسان به این تغییرات حساس نیست. نوعا از یک گونه باید پنج تا ده برابر بطور اضافی موجود باشد تا رنگ آن گونه به چشم بیننده یک رنگ غالب به نظر آید. افزایش بیشتر در این نسبت هیچ تاثیر قابل روئیتی ندارد. فقط در ناحیهای که نسبت از پنج تا ده برابر برای یک شکل به نسبت مشابهی برای یک شکل تغییر کند، بنظر میآید که رنگ محلول تغییر کرده است.
پس ، تغییر رنگ صوری شامل یک تغییر عمده در وضعیت تعادل شناساگر است. بعضی از شناساگرها نیاز به تغییر نسبت کمتری دارند و بعضی دیگر ، به تغییر بیشتر. بعلاوه ، تفاوت قابل توجهی نیز در توان افراد مختلف جهت تشخیص رنگ وجود دارد. در حقیقت ، شخص مبتلا به کور رنگی ممکن است قادر به تشخیص هیچ گونه تغییر رنگی نباشد.
دامنه PH برای تغییر رنگ
ادامه مطلب ...کتون ها
کتون ها

R۱(CO)R۲
اتم کربن که با دو اتم کربن پیوند دارد آن را از گروههای عاملی کربوکسیلیک اسیدها ، آلدهیدها، استرها، آمیدها و دیگر ترکیبهای اکسیژندار جدا میکند. پیوند دوگانهٔ گروه کربونیل نیز کتونها را از الکل ها و اترها باز میشناساند.
به کربنی که به کربن گروه کربونیل چسبیده کربن آلفا و به هیدروژنی که به این کربن چسبیده هیدروژن آلفا گویند. در حضور یک کاتالیزور اسیدی کتون به keto-
آنزیمها و امولسیفایرها
● فناورینانولولههای کربنی ▪ غشاهای نانولولهای
نانولولههای کربنی میتوانند برای تشکیل غشاهایی با تخلخل نانومتری و دارای قابلیت جداسازی آلودگیها، به طور یکنواخت همراستا شوند. تخلخلهای نانومتری نانولولهها این فیلترها را از دیگر فناوریهای فیلتراسیون بسیار انتخابپذیرتر نموده است. همچنین نانولولههای کربنی دارای سطح ویژه بسیار بالا، نفوذپذیری زیاد و پایداری حرارتی و مکانیکی خوبی هستند. اگر چه چندین روش برای سنتز نانولولههای کربنی استفاده شده است، غشاهای نانولولهای میتوانند به وسیله پوششدهی یک ویفر سیلیکونی با نانوذرات فلزی به عنوان کاتالیست، که موجب رشد عمودی و فشردگی بسیار زیاد نانولولههای کربنی میشود، سنتز شوند و پس از آن برای افزایش پایداری، فضای بین نانولولههای کربنی را با مواد سرامیکی پر نمود.
▪ حذف آلودگیها
مطالعات آزمایشگاهی نشان میدهد که غشاهای نانولولهای میتوانند تقریباً همه انواع آلودگیهای آب را حذف کنند؛ این آلودگی شامل باکتری، ویروس، ترکیبات آلی و تیرگی است. همچنین این غشاها نویدی برای فرایند نمکزدایی و گزینهای برای غشاهای اسمز معکوس هستند.
▪ مقدار تصفیه آب
اگر چه تخلخل نانولولههای کربنی به طور قابل توجهی کوچک است، غشاهای نانولولهای نشان دادهاند که به خاطر سطح داخلی صاف نانولولهها، شدت جریان بیشتر یا یکسانی نسبت به تخلخلهای بسیار بزرگتر دارند.
▪ هزینه
با توسعه روشهای جدید و بسیار مؤثر برای تولید نانولولههای کربنی، هزینه تولید غشاهای نانولولهای به طور پیوسته کاهش مییابد. بر اساس پیشبینی برخی منابع، به دلیل کاهش قیمت نانولولههای کربنی، غشاهای نانولولهای بسیار ارزانتر از سایر غشاهای فیلتراسیون، غشاهای اسمز معکسوس، سرامیک و غشاهای پلیمری خواهد شد. از آن جا که نانولولههای کربنی شدت جریان بالایی را نشان میدهند، فشار مورد نیاز برای انتقال آب نسبت به فرایند نمکزدایی با اسمز معکوس، کاهش مییابد و به دلیل این ذخیره انرژی، نمکزدایی با استفاده از فیلترهای نانولولهای بسیار ارزانتر از اسمز معکوس خواهد بود. انتظار میرود غشاهای نانولولهای بسیار بادوامتر از غشاهای متداول باشند و استفاده مجدد از آنها بازدهی فیلتراسیون را کاهش ندهد.
▪ روش مصرف
غشاهای نانولولهای میتوانند در گزینههای مشابهی به عنوان غشاهای میکروفیلتراسیون و اولترا فیلتراسیون استفاده شوند. مطالعات نشان میدهد که این مواد بادوام و در برابر گرما مقاومند و تمیز کردن و استفاده مجدد از آنها ساده است و با استفاده از فرایند اولتراسونیک و اتوکلاو درC ْ۱۲۱ در مدت ۳۰ دقیقه تمیز میشوند.
▪ توضیحات تکمیلی
انتظار میرود در پنج الی ده سال آینده، شاهد ورود غشاهای نانولولهای نمکزا به بازار باشیم. اخیراً محققان برای غلبه بر چالشهای مرتبط با افزایش مقیاس فناوری، فعالیتهای تازهای را مدنظر قرار دادهاند.
● نانوغربالها
کرمهای ضدآفتاب نانویی چگونه کار میکنند
صنایع آرایشی از اکسیدهای غیرآلی، نظیر اکسید روی و تیتانیم، استفاده میکنند، اما استفاده از این اکسیدها به علت خاصیت سفیدکنندگی روی پوست محدود است. سفیدی به طور مستقیم با پخش نور رابطه دارد. به طور کلی با کاهش اندازهٔ ذرات، شاهد افزایش جذب نور ماوراء بنفش توسط ذرات (به علت عبور کمترِ اشعهها از بین ذرات) و کاهش پدیدهٔ سفیدی (به علت کاهش پدیدهٔ پخش نور) هستیم. بهتازگی روشهای گوناگون برای تولید نانوذرات، توسعه یافته و بر صنعت کرمهای ضدآفتاب اثر گذاشتهاند.
● سفیدی

شکل 1: شمای نور عبوری و انعکاسیافته از یک لایه نازک
۱. عبور نور که منجر به گذشتن آن از ماده بدون هیچ تأثیر متقابلی است؛
۲. نورِ نافذ که منجر به پخش نور میشود؛
۳. انعکاس نور از سطح، مانند آنچه در آینه رخ میدهد؛
۴. انعکاس نفوذی که منجر به پخش نور از سطح میشود.
● پخش نور و اندازهٔ ذرات
شدت نور پخششده به وسیلهٔ یک تکذره، تابعی از اندازهٔ ذره است. با افزایش اندازهٔ ذرات، نور مرئی به علت برخورد با ذرات پخش میشود و با برگشت نور به چشم، ذراتْ سفید دیده میشوند. بنابراین، برای کاهش تأثیر سفیدی، کاهش اندازهٔ دانه راهی است بسیار مؤثر.
آمالگام و ترکیبات آن
مینای دندان یکی از سختترین مواد موجود در این کره خاکی است. دندانهای ما به کمک ما میآیند که انواع و اقسام خوراکیها از سخت تا نرم را بجویم و له کنیم و تحویل دستگاه گوارشمان بدهیم. بجز موارد بسیار محدودی که بهعنوان نواقص مادرزادی محسوب میشوند، دندانهای ما در بدو رویش،سفید،محکم و سالم هستند و به خوبی برای انجام وظایف خود آمادهاند. اگر از دندانهایمان به خوبی مراقبت کنیم، همراهان خوبی برای ما خواهند بود اما با کملطفیهای ما، نظیر عدم رعایت بهداشت و تغذیه نامناسب، باکتریهای دهانی ایجادکننده پوسیدگی دندان، فرصت خوبی پیدا خواهند کرد که مواد غذایی مناسب را تخمیر کرده، اسیدی تولید کنند که این اسید میتواند مینای سخت دندان را حل کرده و پوسیدگی ایجاد کند. پوسیدگیهای دندانی از نقاط بسیار کوچک و معمولا بهصورت لکههای سفید رنگی بر روی دندانها آغاز میشود که در این مرحله، اگر به خوبی از دندانها مراقبت شده و فلوراید از طرق مختلف از جمله دهانشویهها و خمیر دندانها به این لکه سفید برسد،پوسیدگی ممکن است متوقف شود. اما اگر
آشکار سازهای کروماتوگرافی
آشکارساز هدایت گرمایی ( T.C.D) :
اساس این آشکارساز بر روی درجه از دست دادن حرارت از فیلامانها به گاز اطراف خود می باشد و از دست دادن حرارت بستگی به ترکیب گاز دارد. هدایت حرارتی اغلب ترکیبات آلی از گاز حامل بیشتر است. در اثر گرم شدن سیم پیچها شدت جریان عبوری کاهش می یابد.
عوامل موثر در حساسیت آشکارساز :
1- جریان الکتریکی : هر چه جریان بیشتر شود حساسیت زیادتر خواهد شد ولی افزایش بیش از حد باعث سوختن فیلامانها خواهد شد .
2- گاز حامل : هر چه قابلیت هدایت گرمایی گاز حامل بیشتر باشد حساسیت بیشتر خواهد شد به همین جهت گاز هلیم و هیدروژن برای این آشکارساز مناسب می باشد ولی هیدروژن به دلیل قابل انفجار بودن کمتر مورد استفاده قرار می گیرد .
3- درجه حرارت : افزایش شدت جریان باعث افزایش درجه حرارت فیلامانها شده که نتیجه آن افزایش حساسیت آشکارساز می باشد .
رعایت نکات زیر هنگام کار با T.C.D ضروری است :
1- قبل از روشن نمودن آشکارساز گاز حامل را در سرویس قرار داده و از خروج گاز از خروجی آشکارساز مطمئن شوید .
2- هنگام خاموش کردن دستگاه ، ابتدا جریان فیلامانها را قطع کرده اجازه دهید درجه حرارت آشکارساز پایین آید سپس جریان گاز را قطع کنید .
3- هنگام تعویض ستون ، یا Septum و یا هر تغییر دیگر جریان عبوری از فیلامانها را قطع کنید چون وجود اکسیژن باعث اکسیده شده فیلامانها گشته ، حساسیت آشکارساز را کم خواهد کرد .
4- تزریق نمونه هایی نظیر اسید کلرید ریک ، الکیل هالیدها وترکیبات خورنده به آشکارساز صدمه خواهد زد .
آشکارساز یونیزاسیون شعله ای : ( F.I.D)
اساس این آشکارساز برروی قابلیت هدایت الکتریکی گاز که بستگی به ذرات باردار دارد قرار دارد . گاز خروجی از ستون همراه با نمونه بین دو الکترود وارد شده ، یونیزه می شوند .
اکثر ترکیبات آلی هنگامی که در دمای شعله هیدروژن-هوا، گرماکافت میشوند، واسطه های یونی تولید میکنند که مکانیسمی را در اختیار میگذارند که توسط آن الکتریسیته میتواند از درون شعله عبور کند.
عمل یونیزاسیون در شعله بدرستی روشن نیست و ممکن است یکی از حالتهای زیر اتفاق بیافتد .
1- تشکیل یون H3O + و اگزوترمیک بودن فعل و انفعال باعث عمل یونیزاسیون می شود.
2- یونیزاسیون توسط شعله ایجاد شده در آشکارساز .
3- تشکیل رادیکال آزاد که اگزوترمیک می باشد باعث عمل یونیزاسیون می شود . به هر حال در اثر یونیزاسیون یک میکرو جریان به وجود آمده که پس از تقویت توسط یک الکترومتر به صورت یک سیگنال به ثبات فرستاده می شود .
فاصله بین دو الکترود مانند یک مقاومت متغیر عمل کرده و مقدار مقاومت از روی تعداد ذرات باردار معین می شود . شعله ایجاد شده در این آشکارساز حاصل مخلوط هوا و هیدروژن می باشد . ناخالصی های موجود در گاز حامل و bleeding ستون همیشه یک جریان ثابتی از ذرات باردار بین دو الکترود ایجاد می نماید که به جریان زمینه موسوم می باشد که معمولا برای حذف این جریان از Bucking Votlage استفاده می شود تا خط مبدا بدون پارازیت باشد . برای استفاده از این آشکارساز در ماکزیمم حساسیت ،
نیاز به بهینه کرده سرعت جریان گازهای هوا و هیدروژن می باشد که معمولا هیدروژن و هوا می باشد و دامنه خطی آشکارساز 107 می باشد .
آلوده شدن FID و تمیز کردن آن :
آلودگی در این آشکارساز به سه دسته تقسیم می شوند ؛
1- آلوده شدن توسط فاز مایع
2- آلوده شدن در اثر استفاده از حلالهایی نظیر بنزن و تولوئن
3- آلوده شدن توسط آب
فازهای مایع سیلیکونی به دلیل تشکیل SiO2 در شعله باعث آلوده شدن این آشکارساز شده و وجود ذرات SiO2 در قسمتهای Jet , Collector Ion سبب نوساناتی در خط مبدا خواهد شد در چنین مواردی باید دتکتور را باز کرده قسمت های آلوده شده را با حلال مناسب و یا سمباده نرم تمیز نمود .
استفاده از حلالهایی نظیر بنزن و تولوئن در شعله ایجاد دوده نموده و آلوده شدن قسمتهای مختلف سبب نوساناتی در خط مبدا خواهد شد که باید آشکارساز تمیز گردد .
در صورت پایین بودن درجه حرارت آشکارساز آب تشکیل شده در شعله آنرا آلوده کرده که برای رفع آن کافی است درجه حرارت آشکارساز بالاتر از 120°c انتخاب شود .
مبردها
برای انتقال حرارت از داخل یک محفظه یا اتاق به خارج , احتیاج به یک واسطه است. در یک سیستم سرد کننده مکانیکی استاندارد , عمل گرفتن حرارت با تبخیر مایعی در دستگاه تبخیر (Evaporator), و پس دادن آن در دستگاه تقطیر (Condenser) صورت می گیرد و این امر باعث تغییر حالت ماده سرمازا از بخار به مایع می گردد .مایعاتی که بتوانند به سهولت از مایع به بخار و بالعکس تبدیل شوند به عنوان واسطه انتقال حرارت به کار برده می شوند, زیرا این تغییر حالت باعث تغییر حرارت نیز می گردد .برخی از این مواد سرمازا از مواد دیگر مناسب تر هستند .
خصوصیات مواد سرمازا :
سیالی که به عنوان ماده سرمازا مورد استفاده قرار می گیرد باید دارای کیفیات زیر باشد:
1- سمی نباشد.
2- قابل انفجار نباشد .
3-اکسید کننده نباشد .
4- قابل اشتعال نباشد .
5- در صورت نشت به سهولت قابل تشخیص باشد
6- محل نشت آن قابل تعیین باشد .
7- قادر به عمل کردن در فشار کم باشد (نقطه جوش پایین) .
8- از نوع گازهای پایدار باشد .
9- قسمت هایی که در داخل مایع حرکت می کند به سهولت قابل روغنکاری باشند.
10- تنفس کردن آن مضر نباشد .
11- دارای گرمای نهان متعادلی برای مقدار تبخیر در واحد زمان باشد .
12- جابجایی نسبی آن برای ایجاد مقدار معینی برودت کم باشد .
13- دارای کمترین اختلاف, بین فشار تبخیر و تقطیر باشد .
ماده سرمازا نباید خورنده باشد (ایجاد زنگ زدگی کند) تا ساختن تمام قطعات سیستم از فلزات معمولی با عمر خدمتی طولانی تر عملی گردد.
مبنای مقایسه مواد سرمازای به کار رفته در صنعت سرد کنندگی , بر اساس حرارت تبخیر 5 درجه فارنهایت و حرارت تقطیر 68 درجه فارنهایت است .
شناسایی مواد سرمازا بوسیله شماره گذاری :

